La proteina spike S1, del SARS-CoV-2, induce formazione di fibrinogeno resistente alla fibrinolisi(*): di seguito le implicazioni per la formazione di microcoaguli in COVID-19
Titolo originale: SARS-CoV-2 spike protein S1induces fibrin(ogen) resistant to fibrinolysis: Implications for microclot formation in COVID-19
PREMESSA Proponiamo qui la traduzione parziale di uno studio (preprint) di grande interesse, relativo alla relazione tra i disordini della coagulazione del sangue (varie coagulopatie che causano sanguinamento e trombocitopenia o uno stato di ipercoagulabilità) in rapporto alla proteina spike del virus SC2 . Gli eritrociti del sangue, esposti alla proteina spike, anche a basse concentrazioni, hanno mostrato agglutinazione, piastrine iperattivate, e formazione di microparticelle derivate dalle piastrine. Si sono formati depositi spontanei di amiloide senza necessità di esposizione alla trombina. La proteina spike libera, rilasciata spontaneamente dalla membrana virale, è rintracciabile in molti organi tra cui il cervello. Dopo l’infezione, la cellula ospite può anche rilasciare le subunità S1 contenenti il dominio legante il recettore (RBD). La subunità S1 libera ha effetti dannosi sull’ospite anche senza infezione diretta delle cellule. È tale subunità isolata come focolaio di infiammazione ad essere l’oggetto dello studio che presentiamo.
INVITO Si tenga presente, nel corso della lettura dello studio, come i vaccini a mRNA siano stati progettati per trasformare le cellule umane in fabbriche di spike sintetica, quale antigene attraverso cui addestrare il sistema immunitario dei vaccinati al riconoscimento del virus. Si riporta, perciò, a seguire, l’abstract di uno studio relativo alla presenza della proteina spike nel plasma sanguigno dei vaccinati:
Le proteine della sindrome respiratoria acuta grave coronavirus 2 (SARS-CoV-2) sono state misurate in campioni di plasma longitudinali raccolti da 13 partecipanti che hanno ricevuto due dosi di vaccino mRNA-1273. Undici dei 13 partecipanti hanno mostrato livelli rilevabili di proteina SARS-CoV-2 già il giorno 1 dopo la prima iniezione di vaccino. La clearance della proteina SARS-CoV-2 rilevabile è correlata alla produzione di immunoglobulina G (IgG) e immunoglobulina A (IgA).
Torniamo all’articolo, oggetto della nostra attenzione, di cui proponiamo la traduzione seppure parziale. Eccone l’abstract e a seguire l’introduzione, la discussione dei risultati e le conclusioni. Per la parte relativa a Materiali, metodi e risultati si rimanda allo studio originale.
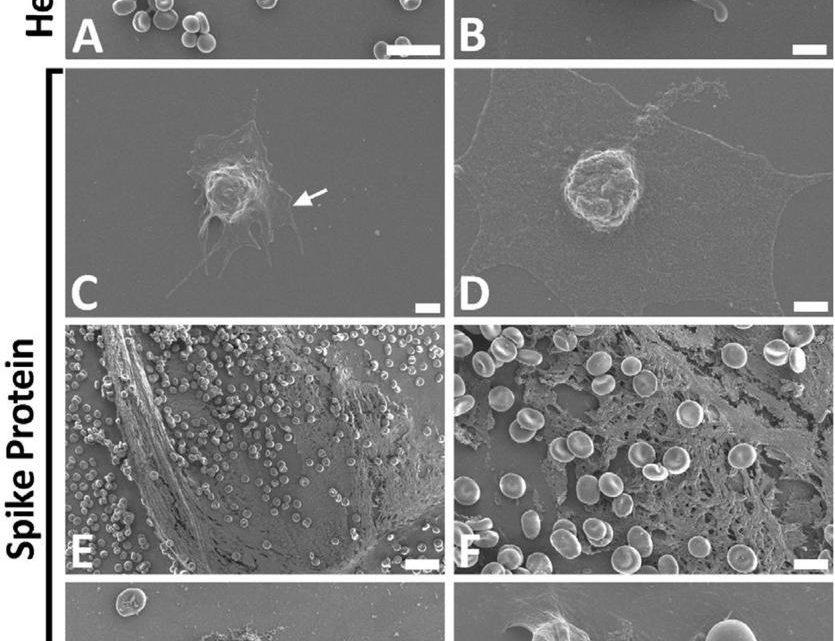
ABSTRACT La sindrome respiratoria acuta grave, infezione indotta da coronavirus 2 (SARS-Cov-2), causa della malattia da coronavirus 2019 (COVID-19), è caratterizzata da patologie cliniche senza precedenti. Una delle patologie più importanti è l’ipercoagulazione e i microcoaguli nei polmoni dei pazienti. Qui studiamo l’effetto della subunità S1 della proteina spike isolata SARS-CoV-2 come potenziale infiammageno sui generis. Utilizzando la microscopia elettronica a scansione e a fluorescenza e la spettrometria di massa, indaghiamo il potenziale di questo infiammageno di interagire direttamente con le piastrine e la fibrina (ogeno) per causare l’ipercoagulazione del sangue. Utilizzando plasma povero di piastrine (PPP), mostriamo che la proteina spike può interferire con il flusso sanguigno. La spettrometria di massa ha anche mostrato che quando la proteina spike S1 viene aggiunta al PPP sano, si verificano cambiamenti strutturali a e fibrina (ogeno), complemento 3 e protrombina. Queste proteine erano sostanzialmente resistenti alla tripsinizzazione, in presenza della proteina spike S1. Qui suggeriamo che, in parte, la presenza di proteine spike in circolazione può contribuire all’ipercoagulazione nei pazienti positivi al COVID-19 e può causare una sostanziale compromissione della fibrinolisi (*). Tale compromissione litica può causare i grandi microcoaguli persistenti che abbiamo notato qui e in precedenza in campioni di plasma di pazienti COVID-19. Questa osservazione può avere un’importante rilevanza clinica nel trattamento dell’ipercoagulabilità nei pazienti COVID-19.
INTRODUZIONE L’infezione indotta da sindrome respiratoria acuta grave da coronavirus 2 (SARS-Cov-2), causa della malattia da coronavirus 2019 (COVID-19), è caratterizzata da patologie cliniche senza precedenti. Le caratteristiche fenotipiche vascolari sono fortemente associate a varie coagulopatie che possono provocare sanguinamento e trombocitopenia o ipercoagulazione e trombosi (Gupta et al., 2020, Perico et al., 2021). Vari biomarcatori della coagulazione infiammatoria circolanti e disregolati, tra cui fibrina (ogeno), D-dimero, P-selectina e fattore von Willebrand (VWF), proteina C-reattiva (CRP) e varie citochine, si legano direttamente ai recettori endoteliali. Le endoteliopatie sono quindi una caratteristica clinica chiave della condizione (Goshua et al., 2020, Ackermann et al., 2020). Durante la progressione delle varie fasi del COVID-19, è probabile che i marcatori della replicazione virale, nonché la deplezione di VWF e fibrinogeno con livelli aumentati di D-dimero e livelli di P-selectina disregolati, seguiti da una tempesta di citochine, siano indicativi di una prognosi sfavorevole (Grobler et al., 2020, Pretorius et al., 2020, Venter et al., 2020, Roberts et al., 2020). Questa prognosi infausta è ulteriormente peggiorata poiché insieme ad una sostanziale deposizione di microcoaguli nei polmoni (Renzi et al., 2020, Ciceri et al., 2020, Bobrova et al., 2020), il plasma dei pazienti COVID-19 porta anche un massiccio carico di coaguli amiloidi preformati (Grobler et al., 2020), e ci sono anche numerose segnalazioni di danni agli eritrociti (Lam et al., 2020, Berzuini et al., 2020, Akhter et al., 2020), piastrine e disregolazione di biomarcatori infiammatori (Grobler et al., 2020, Pretorius et al., 2020, Venter et al., 2020, Roberts et al., 2020).
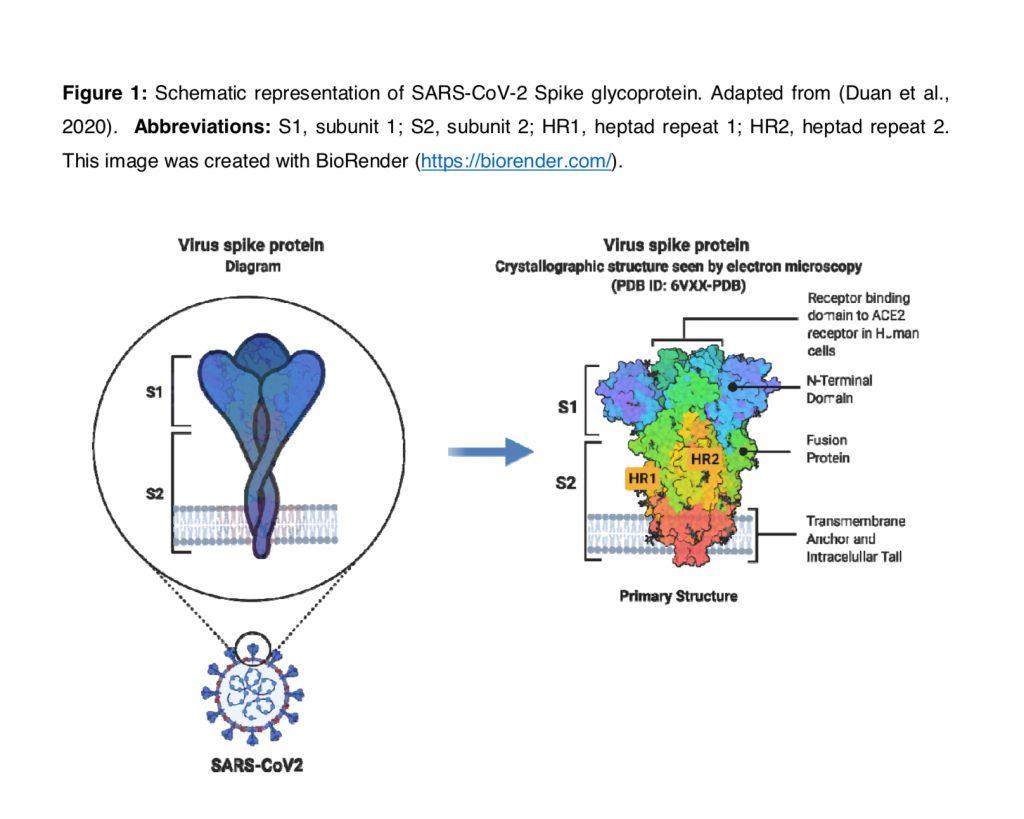
La virulenza del patogeno è strettamente legata alle sue proteine di membrana. Una di queste proteine, che si trova sul virus COVID-19, è la proteina spike, che è una glicoproteina di membrana. Le proteine spike sono i fattori chiave per l’attaccamento del virus alle cellule bersaglio, poiché si legano ai recettori di superficie 2 (ACE2) che convertono l’angiotensina (Bergmann e Silverman, 2020). Le proteine Spike sono proteine di fusione virale di classe I (Kawase et al., 2019). Si presentano come omotrimeri sporgenti sulla superficie virale e mediano l’ingresso del virus nelle cellule ospiti bersaglio (Walls et al., 2020). Una singola proteina spike ha una dimensione compresa tra 180 e 200 kDa e contiene un N-terminale extracellulare, un dominio transmembrana fissato nella membrana del virus e un breve segmento C-terminale intracellulare (Kawase et al., 2019, Zhang et al. ., 2020). Le proteine spike sono rivestite con molecole di polisaccaridi che fungono da camuffamento. Questo aiuta a eludere la sorveglianza da parte del sistema immunitario dell’ospite durante l’ingresso (Zhang et al., 2020). La subunità S1 è responsabile del legame al recettore (Watanabe et al., 2020), con la subunità 2 (S2), una subunità carbossi-terminale, responsabile della fusione e dell’ingresso virale (Flores-Alanis et al., 2020) (vedi Figura 1 ).
Il legame al recettore è certamente responsabile delle patologie cellulo-mediate, ma non spiega di per sé le coagulopatie. La proteina Spike, tuttavia, può essere eliminata ed è stata rilevata in vari organi, compreso il tratto urinario (George et al., 2021). Le proteine S1 possono anche attraversare la barriera ematoencefalica (Rhea et al., 2021). Le particelle S1 libere possono anche svolgere un ruolo nella patogenesi della malattia (Letarov et al., 2020, Buzhdygan et al., 2020). La proteina spike libera può potenzialmente essere rilasciata a causa dello “scatto” spontaneo dei trimeri della proteina S sulla superficie dei virioni e le cellule infette liberano particelle S1 contenenti il dominio legante il recettore libero (Letarov et al., 2020).
Qui studiamo l’effetto della subunità S1 della proteina spike isolata SARS-CoV-2 come potenziale infiammatorio proinfiammatorio sui generis. Indaghiamo il potenziale di questo infiammogeno per interagire direttamente con le piastrine e la fibrina (ogeno) per causare cambiamenti della proteina fibrina (ogeno) e ipercoagulazione del sangue. Determiniamo anche se la proteina spike può interferire con il flusso sanguigno, confrontando campioni PPP sani naïve, con e senza proteina spike aggiunta, con campioni PPP di pazienti positivi al COVID-19 (prima del trattamento). Concludiamo che la proteina spike può avere effetti patologici direttamente, senza essere assorbita dalle cellule. Questo fornisce ulteriori prove del fatto che bersagliarlo direttamente, tramite vaccini o anticorpi, potrebbe essere di beneficio terapeutico.
DISCUSSIONE
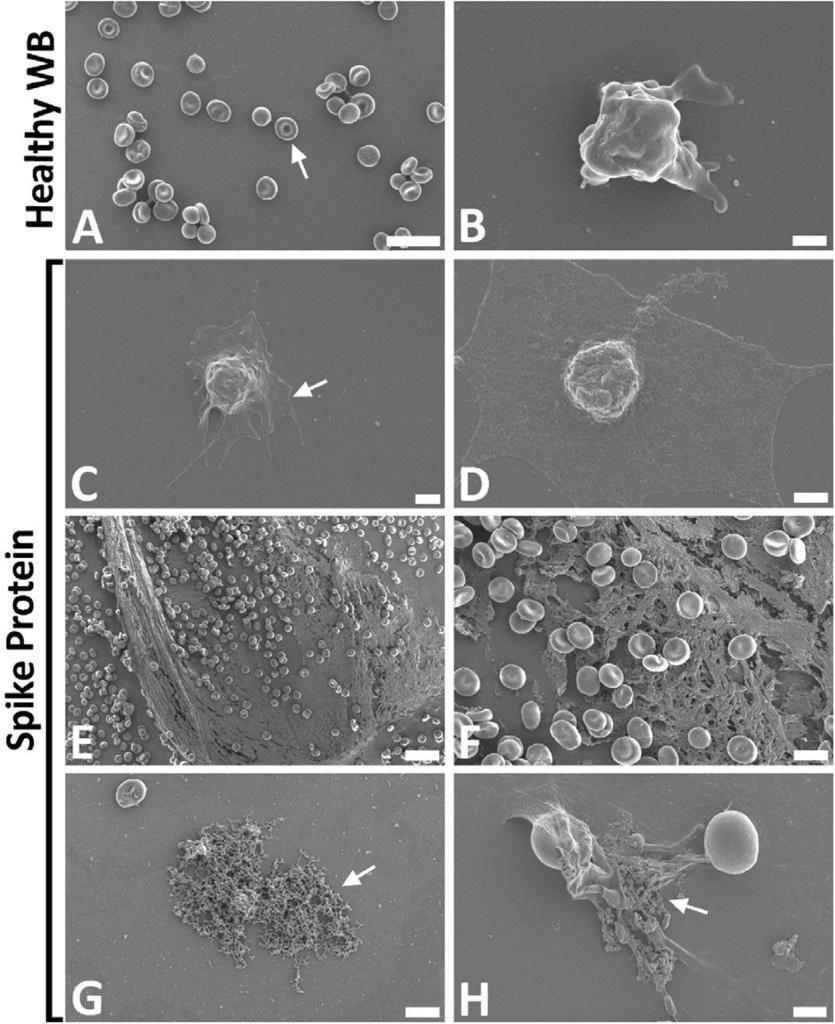
In questa analisi di laboratorio, forniamo la prova che la proteina spike gioca davvero un ruolo importante nell’ipercoagulabilità osservata nei pazienti COVID-19. Causa una coagulazione anomala sia nel fibrinogeno fluorescente purificato che nel PPP, dove è stato dimostrato che la natura dei coaguli è amiloide (ThT come nostro colorante amiloide preferito). Un’osservazione interessante è stata che questi depositi densi sono stati notati sia negli strisci esposti alla proteina spike, sia quando è stata aggiunta la trombina. L’aggiunta di trombina provoca la polimerizzazione del fibrinogeno purificato (Alexa FluorTM488) in reti di fibrina. In genere, queste strutture sono simili a reti (Figura 3A). In presenza di proteine spike, la struttura è cambiata per formare densi depositi di coaguli (Figura 3B). Questi depositi sono stati osservati nel nostro modello di fibrina (ogeno) fluorescente e PPP da individui sani esposti a proteine spike. In PPP sano esposto a proteine spike, seguito da incubazione con ThT, si è verificato un aumento significativo di coaguli anomali di natura amiloide (Figura 4D), rispetto al PPP sanitario. La proteina Spike ha anche causato importanti cambiamenti ultrastrutturali nel WB (come visto con il SEM), dove è stata notata l’iperattivazione piastrinica (Figura 6C e D). Nelle micrografie SEM sono stati osservati anche un aumento della rete di fibrina formata spontaneamente e una formazione anomala di coaguli (Figura 6E – H). Interessante, ampia è stata notata la formazione spontanea della rete di fibrina, senza l’aggiunta di trombina. Ciò è in linea con i risultati pubblicati di recente, in cui abbiamo mostrato un’ultrastruttura simile negli strisci di sangue di pazienti positivi al COVID-19. In questi pazienti sono state osservate anche iperattivazione piastrinica, coagulazione anomala con segnale amiloide e formazione spontanea di fibre di fibrina (Pretorius et al., 2020, Venter et al., 2020).
Con il sistema a flusso microfluidico si sono formati dei coaguli, infondendo trombina nell’intero microcanale, simulando così uno stato di ipercoagulabilità, dove il danno endoteliale era esteso. Dato che il canale di flusso era realizzato interamente in plastica ed era privo di cellule endoteliali, il componente principale in esame era lo stesso PPP (principalmente proteina del fibrinogeno), che, nel caso dei campioni COVID-19, potrebbe aver contenuto effetti a valle di alcune alterazioni endoteliali che darebbero luogo allo stato di ipercoagulabilità caratteristico della malattia. La configurazione del flusso utilizzata in questo studio non è stata in grado di spiegare direttamente i cambiamenti endoteliali, ma ha comunque dimostrato che il COVID-19 provoca anche cambiamenti nel profilo di coagulazione del PPP. Ciò era evidente nel rapido tasso di consumo di trombina e formazione di fibrina nei coaguli COVID-19 e anche nella natura dei coaguli PPP che si erano formati.
I coaguli osservati nel PPP sano con aggiunta di proteine spike erano di particolare interesse in quanto dimostravano un ponte tra coaguli PPP sani e coaguli COVID-19. Come descritto nei risultati, i coaguli PPP sani erano relativamente piccoli e ordinati, mentre i coaguli PPP COVID-19 erano masse grandi e disordinate che si formavano rapidamente e interrompevano il flusso PPP nel canale. I coaguli PPP sani con aggiunta di proteine spike erano una combinazione dei due, che mostravano aree di coaguli agglomerati disordinati, coesistenti con coaguli PPP fibrosi laminari (che erano più grandi dei coaguli PPP sani). Questo stato intermedio può derivare da una serie di fattori, inclusa l’interazione di altri attori biologici che erano assenti dall’impostazione del flusso e il tempo di esposizione alla proteina spike. Ulteriori indagini sarebbero utili per comprendere i meccanismi di coagulazione che vengono alterati in presenza di proteine spike.
Una delle ovvie differenze, che è stata inavvertitamente osservata durante il tentativo di pulire i canali con un flusso d’acqua ad alta velocità (cioè con mezzi meccanici), era la facilità di PPP sano e PPP sano con l’aggiunta di dissoluzione del coagulo proteico spike. Tuttavia, si è verificata una completa incapacità di rimuovere o disturbare i coaguli di PPP COVID-19 dai canali. Dato che la lisi e la dissoluzione del coagulo è una complessa interazione tra fattori biochimici e biofisici, lo studio degli effetti di diversi agenti terapeutici potrebbe chiarire questo fenomeno (Hudson, 2017). Il protocollo di flusso utilizzato in questo studio sarebbe una piattaforma utile per i test diversi trattamenti per l’applicazione clinica. Un’ulteriore limitazione di questa esplorazione è l’uso del PPP nello studio della formazione di coaguli su una scala appropriata alla microcircolazione. Mentre il protocollo consente lo studio dei microcoaguli di fibrina, che sono di interesse per COVID-19, esclude l’influenza dei globuli rossi, che sono noti per influenzare pesantemente il comportamento del flusso sanguigno non newtoniano su quella scala (McHedlishvili, 1998). L’imprecisione del regime di flusso derivante da questa esclusione e dalla variabilità della viscosità introduce errore nei risultati. Tuttavia, l’inclusione del flusso in una scala spaziale appropriata ci ha permesso di osservare la formazione di coaguli PPP COVID-19 nello spazio e nel tempo, in condizioni dinamiche, e ha fornito informazioni che altrimenti si sarebbero rivelate difficili da raccogliere.
La spettrometria di massa ha confermato che la proteina spike provoca cambiamenti strutturali a e fibrina (ogeno), complemento 3 e protrombina. Queste proteine diventano meno resistenti alla tripsinizzazione e cambiano la conformazione, in modo tale che vi sia una differenza significativa nella struttura del peptide prima e dopo l’aggiunta di proteine spike.
CONCLUSIONE
La microscopia elettronica a scansione e a fluorescenza ha rivelato grandi e dense masse anomale e amiloidi nel sangue intero e nel PPP di individui sani in cui ai campioni è stata aggiunta la proteina spike. La spettrometria di massa ha confermato che quando la proteina spike è stata aggiunta al PPP (plasma povero di piastrine), interagisce con le proteine plasmatiche, risultando in fibrina (ogeno), protrombina e altre proteine legate alla coagulazione, per diventare sostanzialmente resistenti alla tripsinizzazione (*), con conseguente riduzione dei frammenti. L’analisi del flusso ha confermato che i microcoaguli possono compromettere il flusso sanguigno. Qui suggeriamo che, in parte, la presenza di proteine spike in circolazione può contribuire all’ipercoagulazione nei pazienti positivi al COVID-19 e può causare una grave compromissione della fibrinolisi. Tale compromissione litica può essere la causa diretta dei grandi microcoaguli che abbiamo notato qui in SEM e microscopia a fluorescenza e precedentemente in campioni di plasma di pazienti COVID-19 (Pretorius et al., 2020, Venter et al., 2020).
A seguire Resia Pretorius, una delle autrici dello studio tradotto
autori
Lize M. Grobbelaar1, Chantelle Venter1, Mare Vlok2, Malebogo Ngoepe3, Gert Jacobus Laubscher 4, Petrus Johannes Lourens4, Janami Steenkamp5 Douglas B. Kell1,67, Etheresia Pretorius1
1Department of Physiological Sciences, Faculty of Science, Stellenbosch University, Stellenbosch, Private Bag X1 Matieland, 7602, South Africa;
2 Central Analytical Facility: Mass Spectrometry Stellenbosch University, Tygerberg Campus, Room 6054, Clinical Building, Francie van Zijl Drive Tygerberg, CAPE TOWN, 7505
3 Department of Mechanical Engineering, Faculty of Engineering and the Built Environment, University of Cape Town, Cape Town, Rondebosch, 7701, South Africa
4Mediclinic Stellenbosch, Stellenbosch 7600, South Africa;
5 PathCare Laboratories, PathCare Business Centre, PathCare Park, Neels Bothma Street, N1 City 7460, South Africa
6 Department of Biochemistry and Systems Biology, Institute of Systems, Molecular and Integrative Biology, Faculty of Health and Life Sciences, University of Liverpool, Crown St, Liverpool L69 7ZB, UK
7 The Novo Nordisk Foundation Centre for Biosustainability, Building 220, Chemitorvet 200, Technical University of Denmark, 2800 Kongens Lyngby, Denmark
(*) Il fibrinogeno, o fattore I della coagulazione è una proteina del sangue contenuta nel plasma, che viene prodotta dal fegato. È uno dei 13 fattori della coagulazione responsabili della cascata coagulativa. Se i risultati degli esami del fibrinogeno sono elevati, il paziente presenta un rischio maggiore di sviluppare coaguli e, nel tempo, di avere un’aumentata predisposizione per le malattie cardiovascolari. — Fibrinolisi Processo per cui la fibrina, in forma di coagulo o di trombo, è enzimaticamente degradata in prodotti solubili (NdA). — La puntura venosa o venipuntura è il processo per ottenere l’accesso endovenoso allo scopo di effettuare una terapia endovenosa o per il prelievo ematico di sangue venoso. La tripsinizzazione è il provoca dissociazione cellulare tramite tripsina, un enzima proteolitico che scompone le proteine.
NOTA come già scritto altrove, certe caratteristiche proprie della spike vaccinale fanno pensar male. In quanto proteina virale essa presenta affinità e coincidenze che ben si adattano alla definizione di arma biologica.
Tuttavia, possiamo sperare che questa ipotesi sia frutto del caso e della fretta, dettata dell’emergenza, non intenzionale. Svilupperemo questa congettura più ampiamente in successive indagini.
articoli correlati a cura dell’autore
Chiare fresche e dolci acque. Con spike o senza?
A te che ti mostri orgoglioso nell’atto di vaccinarti
gironi infernali
Illusioni estive
Futuro cileno o inglese? con Loretta Bolgan e Pedro Morago
Di chi la colpa della morte di queste giovani donne?
Con Pedro Morago Autorizzazione vaccini variazioni sul tema
Penso che si debba interrompere immediatamente la vaccinazione
Le varianti si originano dalle vaccinazioni. Parola di nobel
M. Coppolino – Sars-cov-2 e Covid-19: dall’isolamento del virus alla patologia
Come chiedere aiuto al gruppo FB della Terapia domiciliare precoce covid-19
Vaccini ai civili come già ai militari – Andrea Rinaldelli e la tragica vicenda del figlio Francesco
Un brevetto per il trattamento elettromagnetico della CoV19
La campagna vaccinale di massa crea le condizioni per la sua riproposizione ciclica impedendo l’endemizzazione dell’epidemia
Morte cardiaca improvvisa da vaccini improvvisati?
Idrossiclorochina e Covid-19
Una “misteriosa” malattia? Sarà per caso collegabile alle vaccinazioni di massa!? Ma no! Impensabile….
A cosa serve davvero vaccinarsi?
Nessuna correlazione? Il caso José Baselga
Verso la prima ondata artificiale da vaccino
Seminare domande intervista Loretta Bolgan VACCINI OGM – RISCHI SICUREZZA
La vaccinazione potrebbe prolungare l’emergenza e moltiplicare la sofferenza?
Moltissimo di ciò che ci dicono su virus e vaccini è sbagliato. Il resto è nascosto (seconda parte)
Moltissimo di ciò che ci dicono su virus e vaccini è sbagliato. Il resto è nascosto (prima parte)
La prevenzione vaccinale può essere più pericolosa del covid? Vaccinarsi è un atto di fede?
I “negazionisti” della terapia domiciliare precoce
Dubbi da tamponare
abbasso la mascherina!
Vaccini & autismo
abbasso la mascherina!
Iscriviti per ricevere notifica ad ogni nuovo articolo
canale telegram di Seminare domande
https://t.me/Seminaredomande
© COPYRIGHT Seminare domande
divieto di riproduzione senza citazione della fonte
Non è chiaro se anche le spikes sintetiche originate dai vaccini a mRNA possano causare la medesima problematica